 |
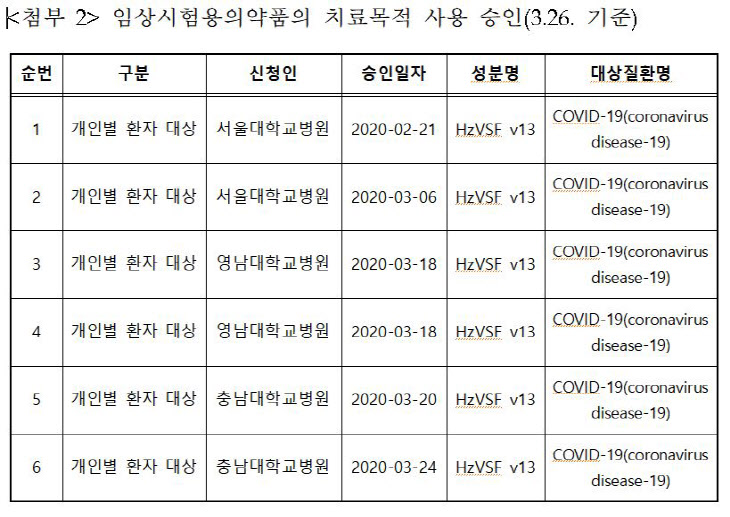
| (자료=식품의약품안전처) |
식품의약품안전처(처장 이의경)은 신종 코로나바이러스 감염증(코로나19) 관련 임상시험 5건과 치료목적 사용을 6건 승인했다고 27일 밝혔다.
식약처는 코로나19 관련 신청된 11건의 임상시험 중 대한감염학회·대한항균요법학회 등 전문가 자문을 거쳐 이 중 5건을 승인했다.
구체적으로 △‘렘데시비르’(에볼라 치료제) 관련 임상시험 3건 △‘칼레트라정’(인체 면역결핍 바이러스(HIV-1) 감염 치료제) △‘히드록시클로로퀸정’(말라리아 치료제) 관련 임상시험 등이다.
인플루엔자 치료제로 임상시험 중인 이뮨메드 치료제 ‘HzVSF v13’를 코로나19 치료 목적으로 사용할 수 있도록 6건을 승인했다. 이 회 10건은 검토 중이다.
치료목적 사용승인이란 생명이 위급하거나 대체치료수단이 없는 응급환자 등의 치료를 위해 의약품으로 허가되기 전의 임상시험용의약품을 식약처 승인을 받아 사용할 수 있도록 하는 제도다.
식약처는 “코로나19 치료제·백신이 신속히 개발될 수 있도록 적극적으로 지원하고, 질병관리본부 등 관련 부처와 긴밀히 협력해 코로나19 치료에 사용되는 의약품이 의료현장에 충분히 공급될 수 있도록 안정적으로 관리해 나가겠다”고 말했다.
송영두 기자 songzio@viva100.com 기자의 다른기사보기 >













